Содержание
- 1 ДИФФЕРЕНЦИАЛЬНЫЙ ПОДХОД К ЛОКАЛЬНОЙ ТЕРАПИИ В СОСТАВЕ КОМПЛЕКСНОГО ЛЕЧЕНИЯ БОЛЬНЫХ С ДОРСОПАТИЕЙ
- 2 Современные подходы к локальной терапии остеоартроза коленных суставов
- 3 Локальная терапия хронических заболеваний опорно-двигательного аппарата.
- 4 Базисная терапия
- 5 Локальная инъекционная терапия при остеоартрозе
- 6 Место локальной терапии в лечении остеоартроза
- 7 Локальная терапия остеоартроза
ДИФФЕРЕНЦИАЛЬНЫЙ ПОДХОД К ЛОКАЛЬНОЙ ТЕРАПИИ В СОСТАВЕ КОМПЛЕКСНОГО ЛЕЧЕНИЯ БОЛЬНЫХ С ДОРСОПАТИЕЙ
Н.А Шостак
Кафедра факультетской терапии им. акад. А.И. Нестерова ГОУ ВПО РГМУ Росздрава
Широкое распространение боли в спине (БС), в том числе у лиц молодого и среднего трудоспособного возраста, обусловливает большое социально-экономическое значение данной проблемы. По этой причине в число приоритетных направлений, рекомендованных ВОЗ к детальному изучению в рамках «Декады костей и суставов» (The Bone and Joint Decade 2000-2010 гг.) отнесены и боли в спине (WHO, 1999) [7].
Вместе с тем многие вопросы диагностики и лечения БС не решены и находятся на стадии обсуждения и изучения. Анализ отечественной и зарубежной литературы показал, что ни мануальная терапия, ни физиотерапия, ни тракция позвоночника и другие методы лечения БС не решили проблему. Хирургическая стабилизация с декомпрессией позвоночника является дорогостоящей процедурой, применяемой лишь у небольшого числа больных с осложненным течением заболевания (грыжи дисков, стеноз позвоночного канала и др.).
Схема. Основные механизмы патогенеза болевого синдрома у пациентов с БС.
Таблица 1. Правила лечения боли в поясничной области
Лечение боли в поясничной области с позиций доказательной медицины основано на следующих правилах [1, 7]:
• больному рекомендуют продолжать обычную повседневную деятельность или как можно скорее возобновить ее (уровень доказательности А);
• больному рекомендуется избегать длительного (более 2 дней) постельного режима (уровень доказательности А);
• эффективность нестероидных противовоспалительных препаратов (НПВП) при БС доказана (уровень доказательности А);
• при острой боли в поясничной области активные физические упражнения в течение первых 2 нед заболевания не эффективны (уровень доказательности В);
• достоверных доказательств эффективности ношения поддерживающего корсета не существует (уровень доказательности С).
Таблица 2. Требования к местным лекарственным препаратам
• Препарат должен быть высокоэффективным при лечении патологии,
то есть обладать анальгетическим действием
• Не должен вызывать местных токсических и аллергических реакций
• Должен проникать через кожу, достигая ткани-мишени
• Концентрация препаратов сыворотки в крови не должна достигать уровня, приводящего к зависимым от дозы побочным эффектам
• Метаболизм и выведение препарата должны быть такими же, как при системном применении
Литература
1. Клинические рекомендации для практических врачей, основанные на доказательной медицине. М., 2001.
2. Насонов Е.Л. Нестероидные противовоспалительные препараты (перспективы применения в медицине). М., 2000.
3. Павлов В.Н., Копьева Т.Н., Слуцкий Л.И., Павлов Г.Г. Хрящ. М., Медицина, 1988.
4. Федин А.И. Дорсопатии (классификация и диагностика). Атмосфера. Нервные болезни. 2002; 2: 2-8.
5. Шеметов Д.А. Клинико-гемодинамические показатели при спондилезе (спондилоартрозе), осложненном болями в нижней части спины, и их динамика в процессе терапии. Автореф. дис. . канд. мед. наук. М., 2001.
6. Borenstein D. Эпидемиология, этиология, диагностическая оценка и лечение поясничной боли. Международн. мед. журн. 2000; 35: 36-42.
7. WHO. Department of noncomunicable disease management. Low back pain iniciative. Geneva, 1999.
- Лечение позвоночника, телефон в Москве: +7(495)777-90-03 (многоканальный), +7(495)225-38-03
- метро Нагатинская, улица Нагатинская, дом 1, корпус 21: +7(495)764-35-12, +7(499)611-62-90,
метро Академика Янгеля, улица Академика Янгеля, дом 3: +7(495)766-51-76.

В случаях копирования материалов и размещения их на других сайтах, администрация сайта будет поступать согласно с законодательством РФ об авторском праве.
Современные подходы к локальной терапии остеоартроза коленных суставов
Опубликовано в журнале:
«Медицинский cовет» №2, 2012г.
Е.С.Цветкова, Л.Н.Денисов, д.м.н.,
ФГБУ «Научно-исследовательский институт ревматологии» РАМН, Москва
Болезни костно-мышечной системы широко распространены во всем мире.
Среди всех заболеваний данной группы остеоартроз (ОА) является наиболее частой причиной временной нетрудоспособности и инвалидности.
Ключевые слова: остеоартроз, костно-мышечная система, суставы, нанотехнологии, пластырь
В среднем ОА страдает почти 10% всего населения и почти половина всех пациентов в мире старше 50 лет [1, 2]. По данным Минздравсоцразвития России, с 2000 по 2009 г. число больных ОА увеличилось более чем в 2 раза и его распространенность (на 100 000 населения) возросла за 10 лет на 51,1%. Это может быть объяснено не только улучшением диагностики, но и увеличением продолжительности жизни и накоплением факторов риска ОА, в т.ч. избыточным весом.
ОА рассматривается как «гетерогенная группа заболеваний различной этиологии со сходными биологическими, морфологическими, клиническими проявлениями и исходами, при которых в патологический процесс вовлекаются хрящ, суб-хондральная кость, связки, капсула, синовиальная оболочка и околосуставные мышцы» [3].
Основным клиническим симптом ОА является боль в суставах различной интенсивности и продолжительности: у 25% больных старше 50 лет боль столь сильна, что не только ограничивает функциональную активность, но и приводит к полной потере трудоспособности [4, 5]. У пожилых пациентов продолжительность жизни зависит в большей степени от интенсивности боли, чем от сопутствующих заболеваний [5].
Основная цель терапии ОА коленных суставов (ОА КС) — минимизация боли и улучшение качества жизни пациентов. Несмотря на значительный прогресс, достигнутый в последние годы в лечении ОА КС, проблема безопасности применяемых лекарственных средств, особенно у больных пожилого возраста, выходит на первый план.
Наряду с системной фармакотерапией в ревматологии широко используются средства локального воздействия на болевые зоны. Появление новых методов местной аналгезии вызывает закономерный интерес.
Последние рекомендации OARSI (Osteoarthritis Research Society International) и Ассоциации ревматологов России по терапии ОА КС регламентируют применение различных групп лекарственных средств, в т.ч. локальных нестероидных противовоспалительных препаратов (НПВП) [6, 7]. Локальные НПВП широко применяются при ОА, однако риск развития системных (желудочно-кишечных и кардиоваскулярных) нежелательных явлений достаточно высок [8, 9, 10]. В связи с этим поиск средств для локальной аналгезии продолжается, поскольку оптимальный лекарственный препарат (или метод) ни прямо, ни косвенно не должен представлять опасность для пациента и требовать постоянного медицинского наблюдения [9].
Относительно недавно в практике врача-ревматолога стала успешно использоваться так называемая трансдермальная терапевтическая система (ТТС) с 5%-ным лидокаином как средство периферической аналгезии при болях в нижней части спины, остеоартрозе и других подобных состояниях. Метод относительно безопасен, местные нежелательные явления отмечены в 5—15% случаев [10].
Особый интерес представляют лечебные пластыри, созданные на основе нанотехнологий, в частности НАНОПЛАСТ форте (НФ), который содержит магнитный слой из редкоземельных металлов и нанопорошок — индуктор длинноволнового инфракрасного излучения и обладает болеутоляющим, миорелаксирующим действием.
К настоящему моменту сравнительного изучения эффективности пластыря НФ не проводилось. В связи с этим целью нашей работы была оценка эффективности, системной и локальной переносимости НФ в сопоставлении с пластырем-плацебо у больных ОА КС.
МАТЕРИАЛЫ И МЕТОДЫ ИССЛЕДОВАНИЯ
В двойное слепое двухнедельное проспективное сравнительное рандомизированное многоцентровое плацебо-контролируемое исследование было включено 120 пациентов с ОА КС I—III рентгенологической стадии по Kellgren и Lowrence. Условием включения в исследование являлось подписание пациентом информированного согласия, а критериями — интенсивность боли в анализируемом («целевом») суставе ≥ 40 мм по визуальной аналоговой шкале (ВАШ), отсутствие клинически значимых нарушений функции печени и почек, прием НПВП в стабильной дозе не менее 4 недель до исследования, адекватная стабильная терапия сопутствующих заболеваний. В исследование не включали пациентов с вторичным ОА, иными ревматическими заболеваниями (РА, ББ и др.), синовитом коленных суставов, требующим введения кортико-стероидов, тяжелыми сопутствующими заболеваниями, поражением кожных покровов в области коленного сустава. Первичным критерием эффективности являлось уменьшение боли в «целевом» коленном суставе (индекс WOMAC, раздел А) на ≥ 50% от исходного уровня. Кроме того, в процессе исследования проводилась в динамике оценка разделов В и С индекса WOMAC; общая оценка лечебного эффекта раздельно больным и врачом в мм по ВАШ, ежедневная оценка больным интенсивности боли в мм по ВАШ.
Суммарная эффективность НФ оценивалась на 14 день раздельно врачом и больным по следующим градациям: 1 — значительное улучшение, 2 — улучшение, 3 — отсутствие эффекта, 4 — ухудшение. Потребность в приеме НПВП контролировалась на протяжении исследования: рассчитывалась суточная доза, фиксировалось уменьшение дозы или полная отмена НПВП в связи с уменьшением интенсивности болевого синдрома.
Переносимость НФ и пластыря-плацебо оценивалась по частоте и выраженности (в баллах от 1 до 3) локальных и/или системных нежелательных явлений. Статистическая обработка полученных результатов проведена с использованием прикладных программ Statistica.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
В исследование в соответствии с кодом рандомизации включено 120 пациентов с ОА КС, по 60 больных в обеих группах. По возрасту, продолжительности ОА, длительности обострения, ИМТ, интенсивности боли в коленных суставах, другим клиническим параметрам и общей активности болезни обе группы были полностью сопоставимы (табл. 1).
Таблица 1.
Начальная характеристика WOMAC и общей оценки пациента и врача
| Показатель | Начальные значения у 120 пациентов. Среднее ± SD (медиана (верхний-нижний квартили)) |
|---|---|
| WOMAC боль (мм) | 237,0 + 87,3 (219[175—294]) |
| WOMAC скованность (мм) | 96,5+48,3 (104 [58—133]) |
| WOMAC функция (мм) | 973,7 + 312,9 (861[688—1030]) |
| WOMAC суммарно (мм) | 1208,3 + 393,1 (1 159[978—1 406]) |
| Общая оценка пациентом (мм) | 58,9 + 15,2 (58[48—67]) |
| Общая оценка врачом (мм) | 46,8 + 16,2 (58[37—57]) |
В целом в анализируемых группах преобладали женщины (97 больных) с ОА КС II—III стадии (93,3%), продолжительностью ОА — 7,7 года и длительностью обострения — 8,9 недели. Среднее значение ИМТ составило 29,5 кг/м 2 . У 55 (73%) больных был диагностирован двухсторонний ОА КС. Из сопутствующих заболеваний наиболее часто (57,5%) отмечалась артериальная гипертензия.
Частота достижения 50%-го уменьшения боли (подшкала А индекса WOMAC) в группе активного НФ была достоверно выше, чем в группе плацебо (38,2 и 16,7% соответственно, р = 0,013; точный критерий Фишера). Интенсивность боли при ходьбе уменьшилась только при использовании активного НФ (р = 0,05; двухфакторный анализ ANOVA), причем достоверное уменьшение боли было отмечено уже на 4-й день применения НФ (рис. 1).

Суммарный показатель боли по индексу WOMAC в основной группе также уменьшился достоверно: с 235,1 до 149,4 мм, что свидетельствует о выраженном анальгетическом эффекте НФ (рис. 2). На фоне лечения в основной группе достоверно уменьшилась утренняя скованность (рис. 3) и увеличилась функциональная активность (рис. 4).

Общее состояние больных по субъективной оценке (р = 0,05) и оценке врача (р = 0,01) улучшилось статистически значимо. Отмена и уменьшение дозы НПВП происходили достоверно (р = 0,007; точный критерий Фишера) чаще в группе больных, применявших активный НФ, чем в группе плацебо: у 23 и 7 пациентов соответственно, т.е. почти у половины больных.
При общей оценке эффективности НФ в основной группе у 82% пациентов отмечалось значительное улучшение. На фоне применения плацебо в 52% случаев эффекта от лечения не было, 5% больных оценили свое состояние как ухудшение.
В группе активного лечения все пациенты полностью завершили исследование. Нежелательных явлений (НЯ), связанных с применением НФ, не выявлено. У 1 пациента зарегистрировано обострение хронического гастрита, что исследователи не связали с использованием НФ. В группе плацебо отмечались ОРВИ (1), гипертонический криз (1), не связанные с применением пластыря-плацебо. Зарегистрированы два локальных НЯ — кожный зуд слабой выраженности и аллергический дерматит, в связи с этим пластырь-плацебо был отменен на 4-й день.
ЗАКЛЮЧЕНИЕ
Таким образом, как отмечено в исследовании Л.Н.Денисова и соавт., высокая анальгетическая активность Нанопласт форте способствует улучшению функциональной активности пациентов с ОА коленного сустава. К достоинствам Нанопласт форте следует отнести его хорошую переносимость и возможность снижения дозы или отмены НПВП на фоне его применения. Пластырь Нанопласт форте может быть рекомендован как в качестве локальной монотерапии, так и в составе комплексного лечения ОА коленного сустава.
Литература:
Полный список литературы вы можете запросить в редакции.
Локальная терапия хронических заболеваний опорно-двигательного аппарата.
Профессор Н.В. Чичасова
ММА имени И.М. Сеченова
- Лечение позвоночника, телефон в Москве: +7(495)777-90-03 (многоканальный), +7(495)225-38-03
- метро Нагатинская, улица Нагатинская, дом 1, корпус 21: +7(495)764-35-12, +7(499)611-62-90,
метро Академика Янгеля, улица Академика Янгеля, дом 3: +7(495)766-51-76.


В случаях копирования материалов и размещения их на других сайтах, администрация сайта будет поступать согласно с законодательством РФ об авторском праве.
Базисная терапия
Базисной терапией ОА обычно обозначают медикаментозное лечение, замедляющее дегенерацию хряща. Применяются препараты, стимулирующие обменные процессы в хряще. Для замедления прогрессирования артроза применяются препараты хондроитинсульфата в дозе 2-3 г в сутки в течение 3 мес и затем 1 г в сутки в течение 3 мес, один курс в год. При применении хондроитинсульфата отмечены диспепсические явления (тошнота, изжога) и аллергические реакции. Отмечен положительный эффект на состояние суставного хряща при введении внутрисуставно препаратов гиалуроновой кислоты курсом по 5-10 инъекций.
Локальная инъекционная терапия при остеоартрозе
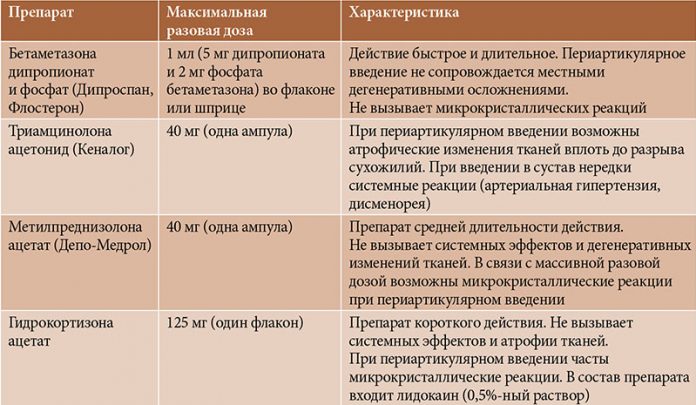
Показания к внутрисуставному и периартикулярному введению глюкокортикостероидных препаратов 1. Активный артрит, особенно с выпотом в полость сустава (при ревматоидном артрите, серонегативных спондилоартритах, системных заболеваниях соединительной ткани и др.). 2. Реактивный синовит различного генеза (при остеоартрозе, подагрическом артрите, травме и др.). 3. Периартриты, тендиниты, тендовагиниты, бурситы, энтезиты и др. — неинфекционного генеза! При определении показаний к локальному введению ГКС-препаратов необходимо учитывать следующие моменты: А. Методика используется предпочтительно при наличии воспаления в ограниченном числе суставов и/или периартикулярных структур. Б. В случае распространенного поражения препарат вводится в наиболее воспаленный(ые) сустав(ы). В. Локальная терапия ГКС-препаратами также показана при необходимости ликвидации (уменьшения) воспаления и болей в суставе или околосуставных мягких тканях у пациентов с противопоказаниями к другим видам терапии (лекарственная аллергия, язвенная болезнь верхних отделов ЖКТ в стадии обострения и др.) или при недостаточной эффективности системного противовоспалительного лечения.
Противопоказания к локальной терапии ГКС-препаратами Абсолютные: 1. Инфекционный (септический) воспалительный процесс в суставе или околосуставных тканях, общее инфекционное заболевание. 2. Патологическая кровоточивость (эндогенная или вызванная применением антикоагулянтов). 3. Отсутствие признаков воспаления в суставе — «сухой сустав», невоспалительный характер боли (например, при остеоартрозе без синовита). 4. Выраженная костная деструкция и деформация сустава (резкое сужение суставной щели, анкилоз), нестабильность сустава как исход артрита. 5. Асептический некроз формирующих сустав эпифизов костей, выраженный околосуставной остеопороз, чрессуставной перелом кости. Относительные: 1. Общее тяжелое состояние пациента. 2. Неэффективность (или кратковременность) действия двух предыдущих инъекций (с учетом нижеуказанных индивидуальных свойств применявшихся ГКС-препаратов).
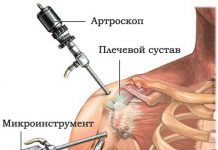
Процедуру проводит врач, владеющий техникой внутрисуставного и периартикулярного введения ГКС-препаратов. Врач нехирургического профиля должен получить специальную подготовку по данной методике и иметь соответствующий сертификат. При выполнении процедуры врачу должна помогать медицинская сестра, владеющая элементами работы операционной сестры. Врач и медсестра одеты в чистые халаты, шапочки и маски. Врач работает в стерильных перчатках, обрабатывая их после каждого больного спиртом. Больной предварительно должен принять душ (ванну) и надеть чистое белье. Предполагаемое место инъекции при необходимости должно быть выбрито.
Место локальной терапии в лечении остеоартроза
Шостак Н.А., Клименко А.А., Кафедра факультетской терапии им. акад. А.И.Нестерова, ГОУ ВПО РГМУ Росздрава
В практике врача-интерниста больные с заболеваниями опорно-двигательного аппарата встречаются достаточно часто. По данным ВОЗ, свыше 4% населения земного шара страдают различными заболеваниями суставов и позвоночника. Более чем в 30% случаев временная нетрудоспособность и в 10% инвалидизация больных связаны с ревматическими заболеваниями.
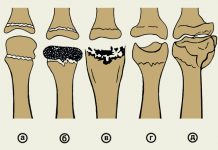
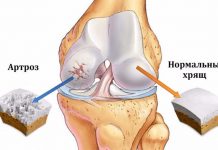
Остеоартроз (ОА) — хроническое прогрессирующее заболевание суставов, характеризующееся первичной дегенерацией суставного хряща с последующим изменением субхондральной кости и развитием краевых остеофитов, сопровождающееся реактивным синовитом.
Заболевание встречается у каждого третьего пациента в возрасте от 45 до 64 лет и у 60-70% — старше 65 лет, причем чаще у женщин (соотношение мужчин и женщин в целом составляет 1:3, а при коксартрозе — 1:7) [1].
| Видео (кликните для воспроизведения). |
ОА — заболевание, развивающееся в результате взаимодействия различных механических и биологических факторов, нарушающих существующее в норме равновесие между процессами деградации и синтеза всех компонентов матрикса, прежде всего в суставном хряще.
В развитии ОА решающее значение придается недостаточному синтезу протеогликанов хондроцитами, а также количественному и качественному нарушению образования протеогликановых агрегатов Важное значение имеет активация матричных протеиназ (коллагеназы, фосфолипазы А2), гиперэкспрессия провоспалительных цитокинов (ИЛ-1 и ФНО-a) и дефицит противовоспалительных цитокинов. Например, трансформирующего фактора роста-b и ингибитора плазминогена-1, которые усиливают катаболические процессы в пораженном хряще. Так, например, ФНО-а имеет рецептор на хондроцитах, является активатором воспаления и тканевого повреждения, стимулируя синтез металлопротеиназ, индуцирует синтез других провоспалительных цитокинов (ИЛ-1, ИЛ-6, ИЛ-8), стимулирует пролиферацию фибробластов и ингибирует синтез коллагена и протеогликанов, что обуславливает его хондродеструктивное действие. Большую роль в патогенезе ОА отводят супероксидным радикалам, уменьшению синтеза синовиоцитами гиалуроновой кислоты, а также гиперпродукции простагландина Е2, который стимулирует активность остеобластов и индуцирует фибропластическую дегенерацию хряща.
Основными клиническими проявлениями ОА являются боль, деформация и тугоподвижность суставов. Кардинальным клиническим симптомом ОА является боль в пораженных суставах. Боль носит неоднородный характер и имеет разнообразные механизмы возникновения.
Типы болей при ОА:
- «Механический» тип характеризуется возникновением боли под влиянием дневной физической нагрузки и стиханием за период ночного отдыха, что связано со снижением амортизационных способностей хряща и костных подхрящевых структур. Это самый частый тип болей при ОА.
- Непрерывные тупые ночные боли (чаще в первой половине ночи) связаны с венозным стазом в субхондральной спонгиозной части кости и повышением внутрикостного давления.
- «Стартовые боли» кратковременные возникают после периодов покоя и проходят на фоне двигательной активности. «Стартовые боли» обусловлены трением суставных поверхностей, на которых оседает детрит — фрагменты хрящевой и костной деструкции. При первых движениях в суставе детрит выталкивается в завороты суставной сумки («суставная мышь»).
- Постоянные боли обусловлены рефлекторным спазмом близлежащих мышц, а также развитием реактивного синовита.
При наличии синовита помимо боли в суставе, как при движении, так и в покое, характерны утренняя скованность, припухлость сустава, локальное повышение кожной температуры. По мере прогрессирования заболевания рецидивы синовита учащаются. Постепенно развиваются деформация и тугоподвижность суставов за счет развития фиброзно-склеротических и гипотрофических изменений параартикулярных тканей. На ранней стадии ОА нарушения функции сустава обусловлены болевым синдромом и рефлекторным спазмом мышц. При прогрессировании заболевания на снижение объема движений влияют сухожильно-мышечные контрактуры, остеофиты и нарушение конгруэнтности суставных поверхностей.
Общая терапевтическая тактика при ОА состоит из трех компонентов [2,
- Механическая разгрузка пораженных суставов
- Купирование синовита
- Предотвращение прогрессирования заболевания
Учитывая выделенные в настоящее время факторы риска прогрессирования ОА (табл. 1), можно сказать что одним из важнейших разделов по лечению больных ОА являются немедикаментозные методы
Таблица 1: Факторы риска прогрессирования ОА
| Факторы риска прогрессирования ОА | Уровень доказательности |
|---|---|
| Коленных суставов: | |
| Низкий уровень образования | C |
| Ожирение | B |
| Снижение мышечной силы | C |
| Продолжительность и тяжесть симптомов ОА | B |
| Рентгенологические признаки ОА, в частности ширина суставной щели | B |
| Наличие варусной или вальгусной деформации | B |
| У женщин в возрасте 40 лет и старше | B |
| Низкий уровень приема с пищей витамина D и низкий уровень акт. вит. D в сыворотке крови | B |
| Тазобедренных суставов: | |
| Низкий уровень образования | C |
| Интенсивная физическая нагрузка во время работы | B |
| Клинические симптомы ОА | C |
| Высокий ИМТ — фактор риска протезирования | B |
| Старший возраст — фактор риска протезирования | C |
| Факторы, препятствующие прогрессированию функциональной недостаточности при ОА | |
| Хорошее ментальное состояние, способность оказывать себе помощь самостоятельно, социальная помощь и выполнение аэробных упражнений | B |
К немедикаментозным методам лечения относят обучение пациента основным аспектам ОА, рекомендации по снижению веса и выполнению физических упражнений. Было показано, что снижение веса у пациентов с ОА коленного сустава приводит к уменьшению боли и улучшению функции сустава, а уменьшение веса на 5 кг или до нормального рекомендованного уровня позволило бы избежать 24% операций на коленном суставе. Пациентам с ОА коленного сустава необходимо выполнять программу физических упражнений, включающую упражнения на укрепление четырехглавой мышцы бедра и увеличение объема движений, а также аэробные нагрузки, занятия в бассейне. Кроме того, пациентам рекомендуется соблюдать следующие правила: ограничить длительное неподвижное стояние и частый подъем по лестнице, избегать положений с упором на колени, с пребыванием на корточках. Для разгрузки пораженных суставов рекомендуется также использование при ходьбе трости, а при выраженной деформации и нестабильности сустава — ортезов, эластичного бандажа или адгезивной повязки.
С целью уменьшения отека и увеличения функциональной активности суставов рекомендуется при гонартрозе использование прерывистого воздействия локальным охлаждением (пакеты со льдом) [10]. Среди физиотерапевтических методов воздействия на симптомы ОА наиболее показано применение переменного магнитного поля низкой частоты, а при неэффективности нестероидных противовоспалительных препаратов (НПВП) чрезкожной электронейростимуляции (ЧЭНС).
Все медикаментозные методы лечения ОА делятся на 3 основные группы: симптом-модифицирующие средства быстрого действия (простые анальгетики, НПВП, опиоидные анальгетики, внутрисуставное введение глюкокортикостероидов, трансдермальные формы лекарств), симптом-модифицирующие средства медленного действия (хондроитин сульфат, глюкозамин сульфат, пиаскледин, препараты гиалуроновой кислоты), структурно-модифицирующие препараты (возможно, к этой группе будут отнесены хондроитин сульфат, глюкозамин сульфат, пиаскледин, стронция ранелат, диацерин) [8].
Центральное место в лечении ОА занимают НПВП, положительное влияние которых на течение ОА определяется их противовоспалительным эффектом и отчетливым анальгетическим действием, что позволяет существенно влиять на выраженность боли в суставах, способствовать разрешению экссудативных явлений и восстановлению объема движений, т.е. воздействовать на наиболее значимые субъективные и объективные симптомы заболевания
Одним из важных компонентов лечения ОА является использование препаратов для местного воздействия. Кроме наиболее часто используемого диклофенака в России зарегистрированы локальные препараты на основе ибупрофена, кетопрофена, индометацина, бутадиона, пироксикама. При назначении того или иного препарата необходимо учитывать концентрацию действующего вещества. Большинство известных препаратов содержат НПВП в концентрации 1%. Необходимо подобрать оптимальную терапевтическую дозу, обеспечивающую анальгетический и противовоспалительный эффект. Низкая концентрация действующего вещества, слабое накопление в зоне воспаления диктуют необходимость многократного нанесения мази или геля на пораженный участок в течение суток. Однако следует отметить, что локальная терапия наиболее эффективна при лечении остеоартроза суставов кистей и коленного сустава [9].
Для усиления локального противовоспалительного эффекта средство должно наноситься многократно в течение дня. Клинические исследования последних лет показали, что минимальным является нанесение локального средства в течение суток. При активном воспалении с максимально выраженными болями нанесение препарата следует увеличить до 6 раз в день. Количество наносимого препарата зависит как от величины сустава, так и от количества пораженных суставов. Поражение крупных суставов (коленных или плечевых) с умеренным болевым синдромом требует нанесения мази или геля в виде полоски до 10 см, тогда как поражение средних суставов (голеностопных, лучезапястных и локтевых) — до 5 см. Средство для местного лечения наносится на область мелких суставов кистей и стоп общим количеством до
Эффективными препаратами признаны мази и гели, содержащие диклофенак, ибупрофен, кетопрофен и пироксикам.
В 1966г. в исследовательской лаборатории фирмы Geigy доктор Alfred Sallmann получил высокоактивное вещество GP 45840, которое вошло в историю ревматологии под названием «диклофенак». В экспериментах на животных было показано, что это действующее вещество обладает выраженными обезболивающими, противовоспалительными и жаропонижающими свойствами [11]. После многочисленных рандомизированных клинических исследований была доказана его высокая эффективность и хорошая переносимость, что сделало диклофенак «золотым стандартом» в ревматологии при лечении многих заболеваний.
В 1986 г. была синтезирована первая форма диклофенака для местного применения — Вольтарен ® Эмульгель ® . Препарат содержит диклофенак-диэтиламмоний, разработанный специально для наружного применения, который в виде геля-эмульсии, соединяющего свойства эмульсии и геля, обеспечивает наиболее эффективное местное лечение боли, воспаления в мышцах, суставах и связках. Уникальная форма Эмульгель ® содержит жировые мицеллы и водно-спиртовой компонент. При нанесении препарата на кожу спиртовой компонент испаряется (это дает легкий охлаждающий эффект), а диклофенак концентрируется в жировых мицеллах, что облегчает его трансдермальное проникновение к очагу боли и воспаления [11, 12].
В 100 граммах жировой эмульсии в водном геле содержится диклофенака диэтиламина 1,16 г, что соответствует 1 г диклофенака натрия. Количество резорбирующегося через кожу диклофенака пропорционально времени контакта препарата и площади, на которую он нанесен, а также зависит от суммарной дозы препарата и степени гидратации кожи. После аппликации на поверхность кожи площадью 500 см2 2,5 г препарата системная абсорбция диклофенака составляет примерно 6%. Применение окклюзионной повязки в течение 10 ч. приводит к троекратному увеличению резорбции препарата.
После нанесения диклофенака в форме Эмульгеля ® на кожу суставов кисти и колена диклофенак определяется в синовиальной оболочке и синовиальной жидкости сустава. В плазме крови его максимальная концентрация примерно в 100 раз ниже, чем после приема диклофенака в форме таблеток внутрь. Чем ближе к коже расположена ткань-мишень, тем выше в ней концентрация препарата [12].
Сравнительно низкая концентрация диклофенака в плазме при местном применении играет решающую роль в обеспечении хорошей переносимости диклофенака в форме Эмульгеля ® , благодаря которой он служит препаратом выбора для лечения пожилых больных с локальными формами ОА.
В большинстве клинических исследований была продемонстрирована высокая эффективность и хорошая переносимость препарата. Особенно в первые 14 дней применения
Также рекомендуется применение фонофореза с диклофенаком в форме Эмульгеля ® , т.к. показано, что использование ультразвукового воздействия увеличивает степень проникновения препарата в ткани и плазменную концентрацию. Например, через 1 час после нанесения Эмульгеля ® у пациентов при использовании ультразвукового воздействия плазменная концентрация препарата составляла 0.0987 мкг/мл в сравнении с концентрацией у пациентов без воздействия ультразвуком 0.0389 мкг/ мл (p=0.01) [17].
Таким образом, несмотря на клиническую форму ОА рекомендуется комплексный подход к лечению заболевания с учетом всех известных медикаментозных и немедикаментозных методов воздействия. Возможность усиления анальгетического и противовоспалительного эффектов может реализоваться через сочетанное назначение пероральных препаратов и локальных форм НПВП, например, диклофенака в форме Эмульгеля ® .
Локальная терапия остеоартроза
В.В. Бадокин, доктор медицинских наук, профессор, А.А. Годзенко, кандидат медицинских наук, Ю. Л. Корсакова, кандидат медицинских наук, РМАПО, Москва
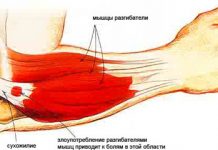
Нестероидные противовоспалительные препараты (НПВП) относятся к одним из самых распространенных лекарственных средств, применяемых в клинической практике. Наиболее широко они используются при лечении воспалительных и дегенеративных заболеваний суставов и позвоночника, микрокристаллических артропатий, диффузных заболеваний соединительной ткани, болезней внесуставных мягких тканей, а также большой группы заболеваний, сопровождающихся болями в нижней части спины, некоторых заболеваний костей. Их широко применяют в кардиологии для профилактики развития тромбозов, воспалительных кардиопатий и для замедления темпов прогрессирования атеросклероза, при посттравматических и послеоперационных болевых синдромах, сопровождающихся воспалением и отеком, при тяжелых приступах мигрени, болезненных menses, почечной и желчной колике, в онкологии для профилактики колоноректального рака и возможного метастазирования злокачественных опухолей.
Основным дегенеративным заболеванием суставов является остеоартроз, который представляет серьезную социально-экономическую проблему и является одной из основных причин стойкой потери трудоспособности. Это заболевание занимает первое место по распространенности среди других ревматических болезней. Оно встречается в популяции у каждого третьего человека в возрасте от 45 до 64 лет и у 60-70% людей старше 65 лет, существенно чаще выявляется у женщин и имеет у них более серьезный прогноз. Соотношение мужчин и женщин в целом составляет 1:3, а при остеоартрозе тазобедренных суставов 1:7. Остеоартроз поражает в первую очередь «нагрузочные» суставы (коленные и тазобедренные), чем значительно ухудшает качество жизни больных.
Наиболее значимыми клиническими проявлениями остеоартроза являются боли в суставах и ограничение в них активных и пассивных движений. Для остеоартроза характерны постепенное начало заболевания, усиление боли в суставах при нагрузке («механический характер боли»), дефигурация суставов за счет небольшого выпота или утолщения синовиальной оболочки, кратковременная утренняя скованность, которая обычно не превышает 30 мин, крепитация или периартикулярный хруст при движениях в пораженных суставах, нестабильность суставных поверхностей с формированием подвывихов, например по типу варусной или вальгусной деформации коленных суставов.
Характерным признаком являются и костные разрастания в области дистальных и проксимальных межфаланговых суставов кистей (узелки Гебердена и Бушара). При остеоартрозе чаще всего встречается поражение коленных, тазобедренных суставов, межфаланговых суставов кистей и 1-го пястнофалангового сустава. Для диагностики этого заболевания большое значение имеют рентгенологические маркеры. К ним относятся: сужение суставной щели, субхондральный остеосклероз, остеофитоз, кистовидные просветления костной ткани, подвывихи, деструкция суставных поверхностей дистальных или проксимальных межфаланговых суставов кистей.
Терапия остеоартроза должна быть комплексной и предусматривать устранение внешних факторов, способствующих его развитию, уменьшение или полное купирование болей в суставах и восстановление их функции, воздействие на проявления реактивного артрита, профилактику дальнейшего его прогрессирования путем коррекции нарушенного метаболизма в гиалиновом хряще.
Медикаментозная терапия представлена двумя основными классами лекарственных препаратов: 1 — симптоматическими препаратами немедленного действия; 2 — препаратами, структурно модифицирующими хрящ. Если 1-я группа препаратов направлена на подавление субъективных проявлений заболевания (боли, утренняя скованность или ограничение подвижности суставов), то 2-я — на замедление темпов его прогрессирования. К быстродействующим симптоматическим препаратам относятся НПВП, простые (неопиоидные) анальгетики и кортикостероиды для внутрисуставного введения, а к структурно модифицирующим — хондропротекторы.
НПВП при остеоартрозе являются основными средствами для проведения симптом-модифицирующей терапии. Их назначение оправдано тем обстоятельством, что хотя остеоартроз и относится к дегенеративным заболеваниям суставов, персистенция воспалительного процесса в тканях сустава наблюдается во всех случаях и локализуется в синовиальной оболочке (синовит), гиалиновом хряще (хондрит) и субхондральной кости (остеит). Персистенция воспалительного процесса в конечном итоге не только усугубляет субъективную и объективную симптоматику остеоартроза, но и способствует прогрессированию структурных изменений при данном заболевании. С этих позиций следует рассматривать позитивное влияние НПВП на течение остеоартроза.
НПВП, которые обладают отчетливым противовоспалительным и анальгетическим действием, позволяют существенно снизить интенсивность и продолжительность болей в суставах, способствовать разрешению экссудативных явлений и восстановлению объема движений, т.е. воздействовать на наиболее значимые субъективные и объективные симптомы остеоартроза.
Разнообразная направленность биологического действия НПВП объясняет не только их противовоспалительное действие, но и большой спектр возможных нежелательных явлений, которые возникают на фоне их приема. Наиболее часто наблюдаются желудочно-кишечные нарушения, проявляющиеся желудочной и/или кишечной диспепсией, развитием эрозивного гастрита и дуоденита, образованием язв желудка и 12-перстной кишки, желудочными кровотечениями. Нередко встречается энтеропатия, коллагеновый колит или рецидивирующий синдром раздраженной кишки, язвы, прободения, стриктуры тонкого и толстого кишечника и кишечные кровотечения. Кроме того, НПВП обладают нефро- и гепатотоксичностью, способствуют задержке жидкости и развитию сердечной недостаточности, артериальной гипертонии, обладают дистрофогенным действием на миокард, воздействуют на метаболизм клеток мозга. Возможны гематологические нарушения вплоть до тяжелых цитопений, торможение агрегации тромбоцитов, аллергические реакции с развитием различных кожных стигматов и бронхообструктивный синдром («аспириновая» астма), что связано с их влиянием на продукцию лейкотриенов.
Класс НПВП включает большое количество препаратов, которые характеризуются общими и отличительными чертами. Они различаются по выраженности анальгетической и противовоспалительной активности, спектру нежелательных явлений, путям введения препарата в организм, областью применения и категорией ингибиции циклооксигеназы (ЦОГ) — основного механизма действия этих фармакологических агентов. К числу наиболее эффективных и хорошо переносимых НПВП относится кетопрофен, производное пропионовой кислоты. К производным пропионовой кислоты также относятся ибупрофен, флурбипрофен, напроксен, тиопрофеновая кислота, фенопрофен, синпрофен. Многие из этих препаратов широко используются в лечении ревматических болезней.
Кетопрофен характеризуется самым быстрым и самым мощным болеутоляющим эффектом среди НПВП. Его анальгетическая активность существенно выше по сравнению с диклофенаком и индометацином. В реализации этого эффекта принимают участие многие физиологические процессы. Так, кетопрофен обладает отчетливой антибрадикининовой активностью, а брадикинин, как известно, понижает порог восприятия боли в очаге воспаления. Кетопрофен подавляет экспрессию ЦОГ-2 в задних рогах спинного мозга и центральной нервной системы (ЦНС), блокирует рецепторы возбуждающих аминокислот и тем самым предотвращает перевозбуждение центральных ноцицептивных структур. Кроме того, он влияет на таламические центры болевой чувствительности, блокируя экспрессию простагландинов в таламусе. Этот препарат обладает также отчетливым противовоспалительным и жаропонижающим действием. Его биодоступность составляет 90% и более.
После локального применения 30 мг кетопрофена в виде пластыря его средняя концентрация становится в 4,4 раза выше в синовиальной оболочке, чем в синовиальной жидкости, и значительно выше в менисках и хряще. При использовании геля кетопрофена (препарат применялся в течение 3-х дней) концентрация в плазме составила 18 нг/мл, в синовиальной жидкости — 1300 нг/мл и капсуле сустава — 2,4 мг/г. Эти данные во многом объясняют лечебное действие кетопрофена при лечении острых и хронических заболеваний суставов.
Особенностью кетопрофена является его удовлетворительная переносимость и высокая безопасность, что было продемонстрировано во многих контролируемых исследованиях. Нежелательные явления, приводящие к отмене препарата при пероральном его применении, встречаются лишь у 3-4% больных и обусловлены преимущественно воздействием на слизистую желудочно-кишечного тракта (ЖКТ).
Частота язвообразования даже при длительном его применении остается примерно такой же, как и при использовании специфического ингибитора ЦОГ-2 — целекоксиба. Сравнительный анализ эффективности и безопасности кетопрофена (200 мг/сут) в сопоставлении с лорноксикамом (16 мг/сут), нимесулидом (200 мг/сут) и целекоксибом (400 мг/сут) у больных остеоартрозом показал достоверное уменьшение всех составляющих индекса WOMAC и снижение СОЭ. Анальгетический эффект при лечении кетопрофеном наступал к 3-4 дню, а при приеме нимесулида, лорноксикама и целекоксиба — только к 7-10 дню.
Медикаментозная гастропатия (гастриты, язвы желудка и/или двенадцатиперстной кишки) чаще всего фиксировалась у больных, принимавших лорноксикам, существенно реже — нимесулид (13,5%) и кетопрофен (13,0%), еще реже — целекоксиб (8,3%). Поражение печени с одинаковой частотой наблюдалось на фоне приема нимесулида и лорноксикама, в то время как терапия кетопрофеном и целекоксибом не вызывала изменения функционального состояния печени. Кетопрофен не приводил к повышению артериального давления (АД) при его суточном мониторировании. Препарат крайне редко вызывает серьезные нефротоксические, кардиотоксические, нейротоксические осложнения. При его применении обычно не развиваются тяжелые аллергические реакции, а общее число побочных реакций не превышает аналогичного показателя у больных, которые принимают селективные ингибиторы ЦОГ-2. Кетопрофен не угнетает продукцию протеогликанов, что очень важно для сохранности хрящевой ткани.
Высокая безопасность кетопрофена доказана результатами анализа крупных европейских многоцентровых исследований, проведенных в Германии и во Франции (в них приняли участие более 64 324 пациентов). Быстрая элиминация кетопрофена (1,5-2 ч) из организма позволяет рекомендовать его больным пожилого возраста без повышения риска возможных побочных реакций.
Одним из препаратов для локальной терапии дегенеративных и воспалительных заболеваний суставов является Быструмгель, содержащий кетопрофен в количестве 25 мг на 1 г геля. Это бесцветный, почти прозрачный гель, pH 5,0-6,0. В его состав входит также трометамол. Использование лекарственной формы для локального применения позволяет избежать возможные нежелательные последствия системного действия НПВП. С другой стороны, применение его при остеоартрозе позволяет существенно увеличить его концентрацию в пораженном суставе.
В проведенном нами открытом рандомизированном сравнительном исследовании изучалась эффективность и переносимость препарата Быструмгель у больных остеоартрозом. В исследование было включено 60 больных, разделенных на 2 группы, сопоставимых по полу, возрасту и длительности заболевания. 1-ю группу составили 30 пациентов, получавших лечение Быструмгелем в дополнение к стандартной терапии, 2-ю — 30 пациентов, получавших стандартную терапию, но без Быструмгеля. Длительность лечения составила 28 дней. Препарат применялся больными ежедневно 2 раза в день, утром и вечером. Он наносился на неповрежденную кожу коленного сустава.
К концу 1-го мес лечения достоверно уменьшилась боль по визуальной аналоговой шкале (ВАШ) у больных 1-й группы (р=0,042). У больных 2-й группы также зарегистрировано улучшение, но оно не было столь выраженным. Наблюдалась положительная динамика и таких показателей, как боль при движении, при ходьбе по ровной местности и ночная боль. У пациентов, принимавших Быструмгель, выявлена положительная достоверная динамика интенсивности боли в положении стоя, чего не отмечено в контрольной группе. Суммарный индекс функциональной способности, который рассчитывался как сумма 13-ти показателей, оцененных по ВАШ, уменьшился к концу лечения в обеих группах, причем различия между началом лечения и его окончанием были достоверны только у больных 1-й группы.
В основной группе пациентов, использовавших Быструмгель, хороший результат терапии зарегистрирован у 83% больных, удовлетворительный — у 16,7%, а в контрольной группе — у 10% и 66,7% соответственно. В 1-й группе не оказалось больных с неудовлетворительным результатом лечения, а во 2-й они составили 23,3%.
Следует отметить хорошую переносимость препарата. У одного больного наблюдался легкий зуд над суставом, который вскоре прошел, что не потребовало отмены Быструмгеля. Местное применение препарата ни в одном случае не привело к гастроинтестинальным осложнениям, а также к гепато-, кардио- и нейротоксичности.
| Видео (кликните для воспроизведения). |
Таким образом, Быструмгель характеризуется высокой противовоспалительной и анальгетической эффективностью у больных остеоартрозом и оказывает длительное лечебное воздействие. Препарат бережно относится к коже и подлежащим тканям как при краткосрочном, так и при долгосрочном применении. Хорошая переносимость и высокая безопасность Быструмгеля позволяют рекомендовать его для наружного применения как больным с остеоартрозом, так и пациентам с воспалительными заболеваниями суставов. При остеоартрозе Быструмгель может применяться как монопрепарат или в качестве составной части комплексной терапии.
Источник: Лечащий врач, 2007 г., № 10.
Источники
Ветрилэ, С. Т. Краниовертебральная патология / С. Т. Ветрилэ, С. В. Колесов. — М. : Медицина, 2016. — 320 c.
Сергей, Владимирович Попов Реология крови при адъювантном артрите / Сергей Владимирович Попов. — Москва: СПб. [и др. ] : Питер, 2011. — 725 c.
Гершбург, М. И. Кинезотерапия от боли в спине. Курс лечебной гимнастики для профилактики и лечения остеохондроза позвоночника / М. И. Гершбург, Г. А. Кузнецова. — М. : Эксмо, 2012. — 192 c.- Николай, Мазнев Артрит, артроз, подагра. Болезни суставов. Авторские методики лечения / Мазнев Николай. — М. : Рипол Классик, Дом. XXI век, 2010. — 389 c.
- Гэлли, Р. Л. Неотложная ортопедия. Позвоночник / Р. Л. Гэлли, Д. У. Спайт, Р. Р. Симон. — М. : Медицина, 2014. — 432 c.


Добрый день! Я работаю ортопедом в государственной поликлинике 11 лет в г. Москва.
Образование: Первый Московский государственный медицинский университет им. И.М. Сеченова;
Специальность: ортопед;
Стаж: 11 лет.